您的当前位置: 网站首页 > 新闻中心 > 新闻资讯 > 详情 行业动态
作者:医药地理 发布时间:2017-02-15 浏览次数: 1563 次 来源:医药网
新年新气象,2017年元月CDE药品注册申请受理数据显示,总量整体上保持平稳,并未如往年一般出现因春节假期因素导致的环比大幅下跌现象。其中新药相关注册受理量相比前一个月还有所增长,特别是在国产化药临床申请和上市申请方面,不仅在数量上继续回升,在品种质量上也有重大突破,新的一年开局可谓良好。
新药临床申请:化药申报持续回暖
综合国产和进口两方面的数据,1月获得CDE受理的新药临床试验申请总计30件(注:同一企业申报同一通用名药物计为1件,下同),其中化药相关21件,生物制品相关8件,中药及天然药物相关1件。对比近半年来的月度数据可以看到,化学新药临床申请量在16年9月跌入谷底后缓慢回升,本月是第4个月保持稳定或上升的态势。
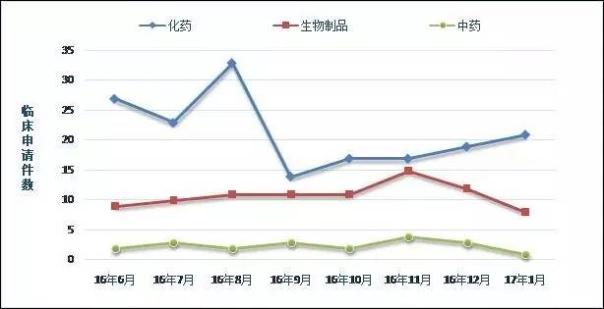
数据来源:中国新药研发监测数据库CPM
本月CDE受理的新药临床试验申请中,包括1类新药11个,其中8个为首次在我国提出临床申请的药物,同时有4家企业新加入1类新药研发阵营,完成了自家首个一类新药的申报(表1)。
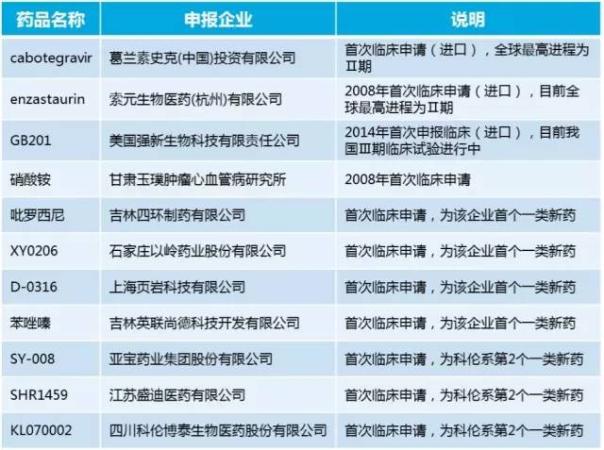
表1. 2017年1月CDE受理临床申请的1类化学新药
新药上市申请:1类新药丹诺瑞韦受瞩目
1月获得CDE受理的新药上市申请总计9件(表2),为近一年来月度受理量平均值的近2倍。其中,国产新药上市申请4件,包括1类新药丙肝治疗药物丹诺瑞韦、2.2类改良性新药格列齐特缓释胶囊和磷酸钠盐散以及生物制品聚乙二醇化重组集成干扰素变异体注射液。其中丹诺瑞韦为治疗丙肝的直接抗病毒药物(DAA),由研发型药企歌礼药业以专利许可的方式从跨国药企罗氏制药引进。如最终能顺利上市,对国内丙肝药物市场以及国内新药研发模式创新均具有重要意义。
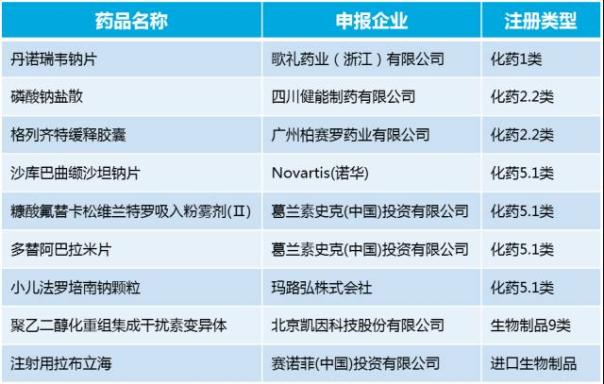
表2. 2017年1月CDE受理新药上市申请
仿制药注册申请:新3类创下新高
1月获得CDE受理的仿制药申请总计27件,环比基本持平。其中按照化药新注册分类申报新3类仿制药注册申请有8件,创下自16年8月首次出现以来的新高(表3)。
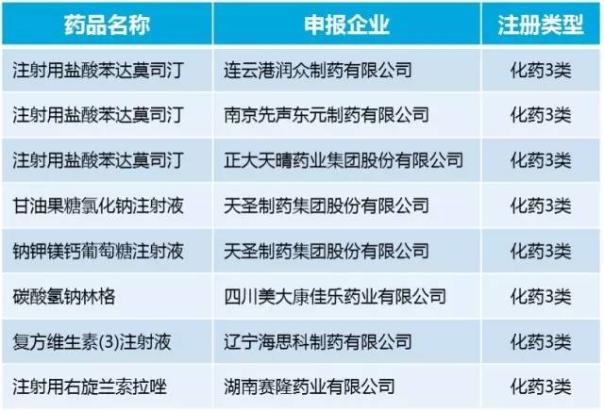
表3. 2017年1月CDE受理新3类仿制药
热门推荐